中考物质分类及复习方法(中考必备单元知识汇总第三单元物质构成的奥秘)
第三单元 物质构成的奥秘

一、分子与原子
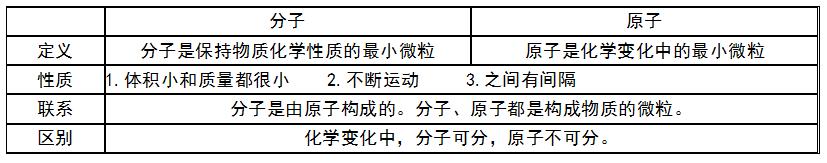
化学变化的实质:分子破裂为原子,原子重新组合成新的分子。
二、原子的构成
1.能画出1-20号原子结构示意图。
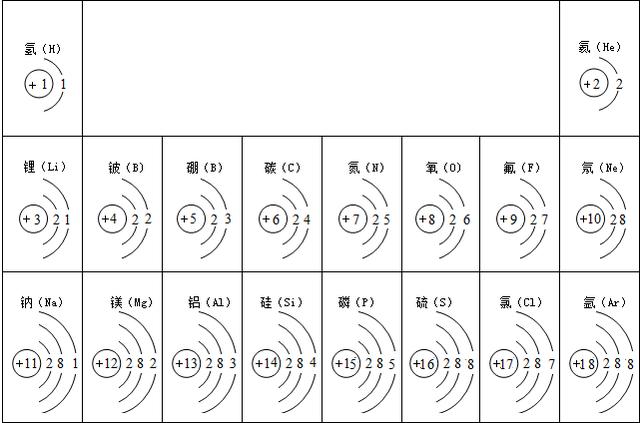
2.在原子中核电荷数=质子数=原子序数=核外电子数。
3.决定元素种类的是质子数,元素化学性质和最外层电子数的关系最为密切。
4.原子的质量主要集中在原子核上,相对原子质量≈质子数 中子数。
5.说明:最外层电子数相同,化学性质不一定相似(如Mg,He最外层电子数都为2)。
最外层电子数不同,其化学性质也有可能相似(如He,Ne均为稳定结构)。
三、元素
1.定义:具有相同核电荷数(质子数)的一类原子的总称。一种元素与另一种元素的本质区别:质子数不同。
2.由同种元素组成的物质不一定是单质,也可能是混合物,(如由O2、O3组成的混合物或金刚石与石墨的混合物),但不可能是化合物。
3.表示方法——元素符号
(1)书写方法:一个字母必须大写,有第二个字母要小写。
(2)意义:表示某种元素 、表示该种元素的一个原子。 如O: 氧元素 、一个氧原子。
注意:有些元素符号还可表示一种单质。 如Fe、He 、C 、Si(由原子直接构成)。
在元素符号前加上数字后只有微观意义,没有宏观意义。如3O:只表示3个氧原子。
(3)元素周期表--门捷列夫。

横行--周期。同一周期的原子,电子层数相同,最外层电子数从左到右依次增加,所以化学性质呈周期性变化。
纵行--族。同一族的原子,电子层数从上到下依次增加,最外层电子数相同,所以化学性质相似。
(4)分类
金属元素:如Mg、Al,最外层电子数特点:<4
非金属元素:如N、C,最外层电子数特点:≥4
稀有气体元素:如He、Ne。最外层电子数特点:2或8
(5)属于同种元素的微粒,质子数一定相同,电子数不一定相同。如钠原子和钠离子。
质子数相同的微粒,不一定属于同种元素。
※四、质子数相同的微粒
1. 可能是两种分子。如 H2O 和 CH4 ;
2.可能是一种分子和一种原子。如 O2 和 S 、 H2O 和 Ne ;
3.可能是一种分子和一种离子。如 O2 和 S2- ;
4.可能是一种离子和一种原子。如 OH- 和 F ;
5.可能是两种离子。如 OH- 和 F- ;
五、离子:带电的原子或原子团
1.表示方法及意义:如Fe3 :一个铁离子带3个单位正电荷。
2.离子结构示意图

注意:与原子结构示意图的区别:质子数=电子数,则为原子结构示意图。质子数≠电子数,为离子结构示意图。
质子数>电子数 则为阳离子,如Al3 质子数<电子数 则为阴离子,如O2-
3.原子和离子的区别与联系

免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com






