过氧化钠与水反应(化学学习氧化钠与过氧化钠)
1,氧化钠的性质
(1)与水反应: Na2O+H2O===2NaOH
(2)与酸性氧化物(如CO2)反应:Na2O+CO2===Na2CO3
(3)与酸(如HCl)反应: Na2O+2HCl===2NaCl+H2O
氧化钠属于碱性氧化物,具有碱性氧化物的通性,反应中化合价不变。
2,过氧化钠的性质
(1)与水反应 2Na2O2+2H2O===4NaOH+O2↑
实验操作:
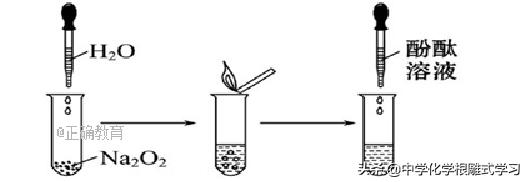
实验现象:
①试管发烫,带火星的木条复燃
②滴加酚酞后溶液先变红,然后再褪色 Na2O2与水反应生成氧气,中间产物过氧化氢具有漂白性.
(2)与二氧化碳反应 2Na2O2+2CO2===2Na2CO3+O2 Na2O2+SO2===Na2SO4(因为二氧化硫具有还原性) 过氧化钠做漂白剂,供氧剂。
(3)与盐酸反应 2Na2O2+4HCl===4NaCl+O2 CO2 以上反应属于歧化反应,过氧化钠中的氧显—1价,容易降到—2价,同时又升高到0价。
过氧化钠主要体现氧化性,是常见的氧化剂及漂白剂。
Na2O2不是碱性氧化物,碱性氧化物是指能与酸反应只生成盐和水的氧化物(反应中化合价不变),Na2O2与盐酸反应时不仅生成NaCl和水,还会有氧气生成(化合价变化了),故不属于碱性氧化物。


免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com