实验室制氧气的探究题(我们周围的空气3)

氧气的实验室制法
今天咱们说氧气的实验室制法,还是先看实验
一、工业制法(分离液态空气法)
原理:利用液态氧和液态氮的沸点不同。——物理变化(蒸馏)
具体过程:
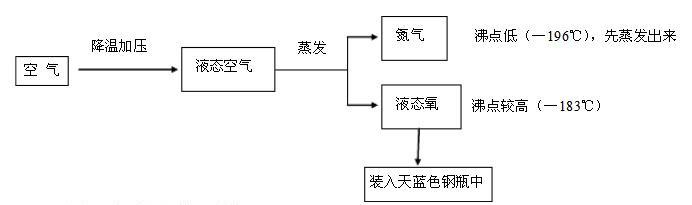
注意:该过程是物理变化
二、实验室制法
1、双氧水(过氧化氢)制取氧气
A、药品:过氧化氢和二氧化锰(黑色粉末 )
B实验原理:

注:MnO2在该反应中是催化剂,起催化作用(在化学反应中能改变其他物质的反应速率(加快或变慢),但本身的化学性质和质量在反应前后没有发生变化的物质。)
C、装置: 固体与液体反应,不需加热(双氧水的为一类)
注意事项:
①、分液漏斗可以用长颈漏斗代替,但其下端应该伸入液面以下,防止生成的气体从长颈漏斗中逸出;
②、导管只需略微伸入试管塞
③、气密性检查:用止水夹关闭,打开分液漏斗活塞,向漏斗中加入水,水面不持续下降,就说明气密性良好。
④、装药品时,先装固体后装液体
⑤、该装置的优点:可以控制反应的开始与结束,可以随时添加液体。 D、步骤:连、查、装(二氧化锰)、定、倒(过氧化氢溶液)、收
装置示意图:

2、用高锰酸钾、氯酸钾制取氧气
A、药品:、高锰酸钾(暗紫色固体)、氯酸钾(白色固体)与二氧化锰(黑色粉末)
B、原理:
①加热氯酸钾(有少量的二氧化锰):

注意:二氧化锰在该反应中是催化剂,起催化作用,不属于反应物。
② 加热高锰酸钾:

实验装置:

C、装置:固固加热装置(加热氯酸钾的为一类)
D、操作步骤:(连)查、装、定、点、收、离、熄。
① 连接装置:先下后上,从左到右的顺序。
② 检查装置的气密性 :将导管的一端浸入水槽中,用手紧握试管外壁,若水中导管口有气泡冒出,证明装置不漏气。松开手后,导管口出现一段水柱。
③ 装入药品:按粉末状固体取用的方法(药匙或纸槽)
④固定装置 :固定试管时,试管口应略向下倾斜;铁夹应夹在试管的中上部
⑤加热药品:先使试管均匀受热,后在反应物部位用酒精灯外焰由前向后加热。
⑥收集气体:
a、若用排水集气法收集气体,当气泡均匀冒出时再收集,刚排出的是空气;水排完后,应用玻璃片盖住瓶口,小心地移出水槽,正放在桌面上(密度比空气大)(防止气体逸出)
b、用向上排空法。收集时导管应伸入集气瓶底部(为了排尽瓶内空气) 用排水法收集时,导管放在集气瓶口
⑦先将导管移出水面
⑧再停止加热
E、易错事项:
a). 试管口要略微向下倾斜:防止冷凝水倒流,使试管底部破裂。药品应平铺在试管底部
b). 导气管伸入发生装置内要稍露出橡皮塞:有利于产生的气体排出。
c). 用高锰酸钾制取氧气时,试管口塞一团棉花:防止高锰酸钾粉末进入导气管,堵塞导管,造成试管炸裂。
d). 排气法收集气体时,导气管要伸入接近集气瓶底部:有利于集气瓶内空气排出,使收集的气体更纯。
e). 实验结束后,先将导气管移出水面,然后熄灭酒精灯:防止水槽中的水倒流,炸裂试管。 F、收集方法:
① 排水法(不易溶于水)
② 向上排空法(密度比空气大)
G、检验、验满
检验:用带火星的木条伸入集气瓶内,发现木条复燃,说明是氧气; 验满:用带火星的木条放在集气瓶口,若木条复燃,证明已满。
,免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com






