高中化学铁铝等金属的性质与应用(金属矿物及铁的冶炼实验讲解)
目前,人类使用的各种金属工具(如铜、铁、铝等)都是金属单质,而自然界中大多数金属(除铂、金、银等外)都是以化合物的形式存在金属矿物中,人类无法使用,如果人类要使用金属工具,就要把金属化合物转变成金属单质,该过程就是金属的冶炼。

1、常见的金属矿物
自然界中大多数金属都是以化合物的形式存在金属矿物中。
常见的金属矿物:铁的矿物、铜的矿物、铝的矿物;
1.1、铁的矿物主要有:赤铁矿(主要成分:Fe2O3)、磁铁矿(主要成分:Fe3O4)、褐铁矿(主要成分:Fe2O3.xH2O)、菱铁矿(主要成分:FeSO4)和黄铁矿(主要成分:FeS2)等;

1.2、铜的矿物主要有:黄铜矿(主要成分:CuFeS2铜和铁硫化物)、孔雀石(主要成分:Cu2(OH)2CO3)、斑铜矿(主要成分:Cu5FeS4铜和铁硫化物)和赤铜矿(主要成分:Cu2O)等;

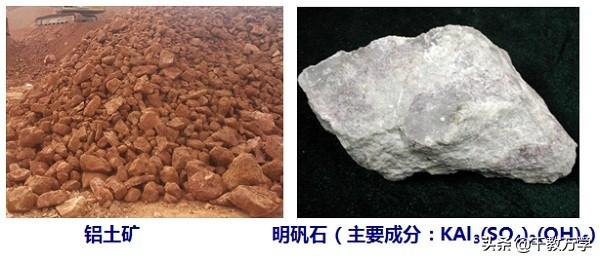
1.3、铝的矿物主要有:铝土矿和明矾石(主要成分:KAl3(SO4)2(OH)6)等;
2、金属的冶炼
金属的冶炼:将金属矿石(金属化合物)转化成金属单质的过程。

2.1、铁的冶炼
铁的冶炼:将铁的化合物转化成单质铁的过程。
例如:工业炼铁原理:氧化铁(Fe2O3)在高温条件下与一氧化碳(CO)反应生成单质铁(Fe)。

纯铁的物理性质:纯铁是银白色金属,熔点为1535℃,密度为7.86g/cm3,质软,有延展性,能被磁铁吸引。

纯铁的化学性质:铁的化学性质比较活泼,能被氧气氧化生氧化铁,和酸会发生置换反应,产生氢气。
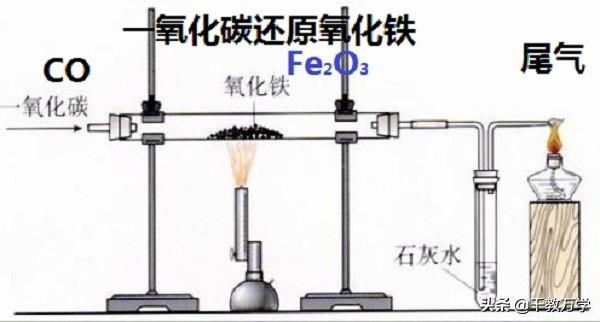
2.2、氧化铁(Fe2O3)在高温条件下与一氧化碳(CO)反应的实验
①实验装置
导管、酒精喷灯、试管、酒精灯、硬质粗玻璃管
②实验步骤
1、组装好设备;
2、向硬质玻璃管中加入红棕色的氧化铁粉末(Fe2O3);
3、先点燃导管末端的酒精灯;
先点燃导管末端的酒精灯目的:防止通入的一氧化碳(CO)气体从导管流出到空气中,引起中毒(一氧化碳与人体的血红蛋白结合,降低了血红蛋白的携氧能力,造成缺氧)
4、通入一氧化碳气体,排出装置内的空气后,再点燃酒精喷灯加热玻璃管中的氧化铁;
5、当红棕色粉末变成黑色时,酒精喷灯停止加热;酒精灯继续燃烧,一氧化碳继续通入;
6、玻璃管中的物质冷却到室温后停止通入一氧化碳,后熄灭导管尾部的酒精灯;
一直通入一氧化碳冷却到室温的目的:防止生成的铁在高温下被空气氧化。
7、将硬质玻璃管中的黑色物质倒在纸上,用磁铁去吸引,再将黑色物质倒入盐酸溶液中观察现象。
③实验观察到的现象与结论
硬质玻璃管中的红棕色粉末变成黑色;
试管中的澄清石灰水变浑浊(说明有二氧化碳气体生成);
黑色物质能被磁铁吸引(说明生成的物质为单质铁);
黑色物质放到盐酸溶液中,有气泡生成,溶液变成浅绿色(说明铁与盐酸反应生成氯化亚铁)。

④实验改进
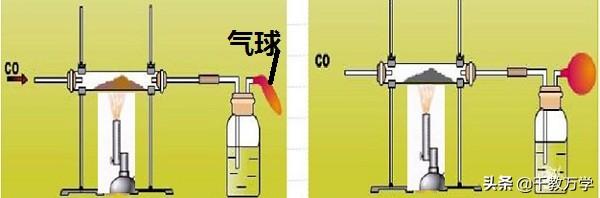
可以将末端的一氧化碳气体通到酒精喷灯的火焰上,减少酒精灯的使用,节约设备,也可以增加酒精喷灯火焰的温度。

导管末端一氧化碳也可用气球来收集。收集的一氧化碳可以再利用。
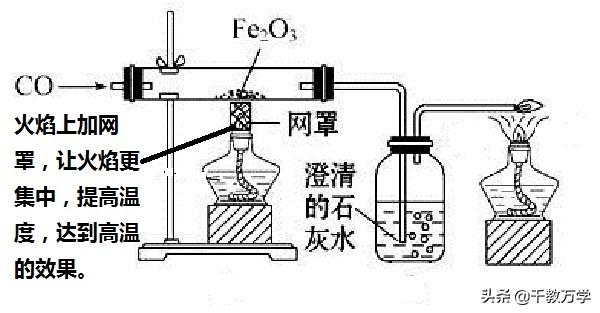
酒精灯火焰上安装灯罩,可以增加火焰的温度,让酒精灯充当酒精喷灯使用。
2.3、工业炼铁
工业炼铁原理:氧化铁(Fe2O3)在高温条件下与一氧化碳(CO)反应生成单质铁(Fe)。

工业炼铁的设备:高炉;
工业炼铁过程:把铁矿石、焦炭、石灰石一起从高炉顶部加入,从下方通入热空气,让焦炭燃烧生成二氧化碳,放出热量,生成的二氧化碳与焦炭在高温下生成一氧化碳气体,一氧化碳气体与氧化铁在高温下反应生成铁。

问题1:高炉中焦炭的作用?

①焦炭燃烧生成二氧化碳,放出热量,提供温度;
②焦炭与二氧化碳在高温下反应生一氧化碳,提供一氧化碳;
问题2:高炉通入热空气的作用?
①节约能量,减少热量损耗;
②为高炉中焦炭燃烧提供氧气;
问题3:高炉加入石灰石的作用?
石灰石作为熔剂,与铁矿石中的杂质反应形成炉渣,更容易除去铁中的杂质。让炼出的铁更纯净。
问题4:高炉中炉渣的出口在生铁的出口的上方?
因为炉渣的密度比生铁轻,炉渣浮在铁水上,炉渣的出口在上方便于炉渣的清理。
,免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com






