高中化学用平衡移动原理解释为(高中化学平衡移动)
一、化学平衡的移动
1.化学平衡的移动
(1)定义
达到平衡状态的反应体系,条件改变,引起平衡状态被破坏的过程。
(2)化学平衡移动的过程

2.影响化学平衡移动的因素
(1)温度:在其他条件不变的情况下,升高温度,化学平衡向吸热反应方向移动;降低温度,化学平衡向放热反应方向移动。
(2)浓度:在其他条件不变的情况下,增大反应物浓度或减小生成物浓度,化学平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,化学平衡向逆反应方向移动。
(3)压强:对于反应前后总体积发生变化的化学反应,在其他条件不变的情况下,增大压强,化学平衡向气体体积减小的方向移动;减小压强,化学平衡向气体体积增大的方向移动。
(4)催化剂:由于催化剂能同时同等程度地增大或减小正反应速率和逆反应速率,故其对化学平衡的移动无影响。
3.勒夏特列原理
在密闭体系中,如果改变影响化学平衡的一个条件(如温度、压强或浓度等),平衡就向能够减弱这种改变的方向移动。
二、外界条件对化学平衡移动的影响
1.外界条件的变化对速率的影响和平衡移动方向的判断
在一定条件下,浓度、压强、温度、催化剂等外界因素会影响可逆反应的速率,但平衡不一定发生移动,只有当v正≠v逆时,平衡才会发生移动。
对于反应mA(g) nB(g)

pC(g) qD(g),分析如下:

2.浓度、压强和温度对平衡移动影响的几种特殊情况
(1)改变固体或纯液体的量,对平衡无影响。
(2)当反应混合物中不存在气态物质时,压强的改变对平衡无影响。
(3)对于反应前后气体体积无变化的反应,如H2(g) I2(g)

2HI(g),压强的改变对平衡无影响。但增大(或减小)压强会使各物质的浓度增大(或减小),混合气体的颜色变深(或浅)。
(4)恒容时,同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响,增大(减小)浓度相当于增大(减小)压强。
(5)在恒容容器中,当改变其中一种气态物质的浓度时,必然会引起压强的改变,在判断平衡移动的方向和物质的转化率、体积分数变化时,应灵活分析浓度和压强对化学平衡的影响。若用α表示物质的转化率,φ表示气体的体积分数,则:
①对于A(g) B(g)

C(g)类反应,达到平衡后,保持温度、容积不变,加入一定量的A,则平衡向正反应方向移动,α(B)增大而α(A)减小,φ(B)减小而φ(A)增大。
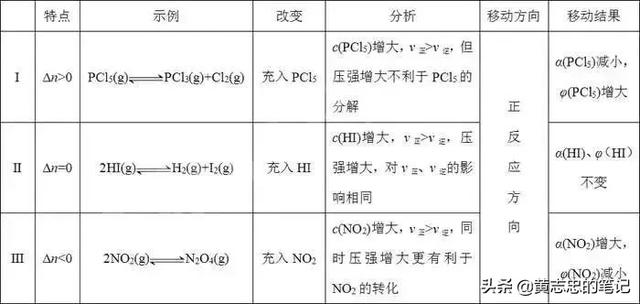
②对于aA(g)

bB(g)或aA(g)

bB(g) cC(g)类反应,达到平衡后,保持温度、容积不变,加入一定量的A,平衡移动的方向、A的转化率变化,可分以下三种情况进行分析:
三、化学平衡图象题的解题方法
化学平衡图象类试题是高考的热点题型,该类试题经常涉及到的图象类型有物质的量(浓度)、速率—时间图象,含量—时间—温度(压强)图象,恒温、恒压曲线等,图象中蕴含着丰富的信息量,具有简明、直观、形象的特点,命题形式灵活,难度不大,解题的关键是根据反应特点,明确反应条件,认真分析图象充分挖掘蕴含的信息,紧扣化学原理,找准切入点解决问题。该类题型在选择题和简答题中都有涉及,能够很好地考查学生分析问题和解决问题的能力,在复习备考中应引起足够的重视。
1.常见的化学平衡图象
以可逆反应aA(g)+bB(g)cC(g) ΔH=Q kJ·mol−1
(1)含量—时间—温度(或压强)图:

(曲线a用催化剂,b不用催化剂或化学计量数a+b=c时曲线a的压强大于b的压强)

(2)恒压(温)线(如图所示):该类图象的纵坐标为物质的平衡浓度(c)或反应物的转化率(α),横坐标为温度(T)或压强(p),常见类型如下所示:

(3)速率−时间图象
根据v−t图象,可以很快地判断出反应进行的方向,根据v正、v逆的变化情况,可以推断出外界条件的改变情况。
以合成氨反应为例:N2(g)+3H2(g)

2NH3(g) ΔH<0。

(4)其他
如下图所示曲线,是其他条件不变时,某反应物的最大转化率(α)与温度(T)的关系曲线,图中标出的1、2、3、4四个点,v(正)>v(逆)的点是3,v(正)<v(逆)的点是1,v(正)=v(逆)的点是2、4。

2.化学平衡图象解答原则
(1)解题思路

(2)解题步骤

以可逆反应aA(g)+bB(g)

cC(g)为例:
(1)“定一议二”原则
在化学平衡图象中,包括纵坐标、横坐标和曲线所表示的意义三个量,确定横坐标所表示的量后,讨论纵坐标与曲线的关系或确定纵坐标所表示的量,讨论横坐标与曲线的关系。如图:

这类图象的分析方法是“定一议二”,当有多条曲线及两个以上条件时,要固定其中一个条件,分析其他条件之间的关系,必要时,作一辅助线分析。
(2)“先拐先平,数值大”原则
在化学平衡图象中,先出现拐点的反应先达到平衡,先出现拐点的曲线表示的温度较高(如图A)或表示的压强较大(如图B)。

图A表示T2>T1,正反应是放热反应。
图B表示p1<p2,A是反应物,正反应为气体总体积缩小的反应,即a+b>c。
四、等效平衡
1.含义
(1)化学平衡状态与建立平衡的条件有关,与建立平衡的途径无关。
(2)对于同一可逆反应,在一定条件(恒温恒容或恒温恒压)下,无论是从正反应(反应物)、逆反应(生成物)或从中间状态(既有反应物、也有生成物)开始,只要建立平衡后,平衡混合物中各组分的比例相同,或各组分在混合物中的百分含量相等,这样的化学平衡互称为等效平衡。
(3)注意只是组分的百分含量相同,包括体积百分含量、物质的量百分含量或质量百分含量,而各组分的浓度不一定相等。
2.审题方法
(1)注意反应特点:反应前后气体的物质的量是否发生变化。
(2)分清平衡建立的条件:是恒温恒压还是恒温恒容。
3.理解等效平衡的意义
(1)对于反应前后气体物质的量有变化的反应,如2SO2(g) O2(g)

2SO3(g)等温等压、等温等容下建立平衡如下图:

容易得出A与C等效,A与D不等效。因为C→D是对反应前后气体体积有变化的反应加压,平衡发生了移动。
结论:对于反应前后气体物质的量有变化的反应,恒温恒压时只要起始加入的物质按方程式化学计量数转化到方程式一侧,比例相同就可建立等效平衡;而恒温恒容时,则需起始加入的物质按方程式化学计量数转化到方程式一侧,完全相同才能建立等效平衡,因为反应物物质的量的变化会引起平衡的移动。
(2)对于反应前后气体物质的量没有变化的反应,如:H2(g) I2(g)

2HI(g)等温等压、等温等容下建立平衡如下图:

容易得出A与C等效,A与D等效。因为C→D平衡不发生移动。对反应前后气体体积不变的反应加压,平衡不移动。
结论:对于反应前后气体物质的量不变的反应,无论是恒温恒压还是恒温恒容,只要加入的物质按方程式化学计量数转化到方程式一侧,比例相同就可建立等效平衡。
五、解答化学平衡移动题目的思维模型

六、构建“虚拟的第三平衡”法解决平衡间的联系
在解题时若遇到比较条件改变后的新、旧平衡间某量的关系有困难时,可以考虑构建一个与旧平衡等效的“虚拟的第三平衡”,然后通过压缩或扩大体积等手段,再与新平衡沟通,以形成有利于问题解决的新模式,促使条件向结论转化,例如:
(1)构建等温等容平衡思维模式:新平衡状态可认为是两个原平衡状态简单的叠加并压缩而成,相当于增大压强。

(2)构建等温等压平衡思维模式(以气体物质的量增加的反应为例(见图示):新平衡状态可以认为是两个原平衡状态简单的叠加,压强不变,平衡不移动。


免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com






