化学反应热的所有知识点(第6章微题型53化学反应热的基本概念和大小比较)

1.(2020·云南临沧第一中学高三期末)下列热化学方程式书写正确的是(ΔH的绝对值均正确)( )
A.2H2O(g)===2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1(反应热)
B.C(s)+O2(g)===CO(g) ΔH=-110.5 kJ·mol-1(燃烧热)
C.C2H5OH+3O2===2CO2+3H2O
ΔH=-1 368.8 kJ·mol-1(反应热)
D.2NaOH(aq)+H2SO4(aq)===Na2SO4(aq)+2H2O(l)
ΔH=-114.6 kJ·mol-1(中和热)
2.(2020·全国高三专题练习)下列说法不正确的是( )
A.已知冰的熔化热为6.0 kJ·mol-1,冰中氢键键能为20 kJ·mol-1,若熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键
B.在一定条件下,某可逆反应的ΔH=+100 kJ·mol-1,则该反应正反应活化能比逆反应活化能大100 kJ·mol-1
C.甲烷的燃烧热为890.3 kJ·mol-1,则1 mol CH4发生反应CH4(g)+2O2(g)===CO2(g)+2H2O(g)放出的热量小于890.3 kJ·mol-1
D.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放出热量19.3 kJ,其热化学方程式可表示为N2(g)+3H2(g)2NH3(g)
ΔH=-38.6 kJ·mol-1
3.(2021·石家庄高三期末)下列说法正确的是( )
A.反应的热化学方程式的书写中,ΔH的大小与化学计量数无关
B.ΔH<0、ΔS<0的反应在高温时能自发进行
C.实验室欲快速制取氢气,可利用粗锌与稀硫酸反应
D.金属表面镀银时,应把镀件作为电镀池的阳极
4.(2020·全国高三专题练习)下列说法中,正确的是( )
A.1 mol H2SO4与1 mol Ba(OH)2反应生成H2O时放出的热叫做中和热
B.ΔH>0表示放热反应,ΔH<0表示吸热反应
C.热化学方程式中的化学计量数表示物质的量,可以是分数
D.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热
5.(2020·内蒙古包头一中月考)分别取50 mL的0.50 mol·L-1盐酸与50 mL的0.55 mol·L-1氢氧化钠溶液混合进行中和热的测定,下列说法正确的是( )
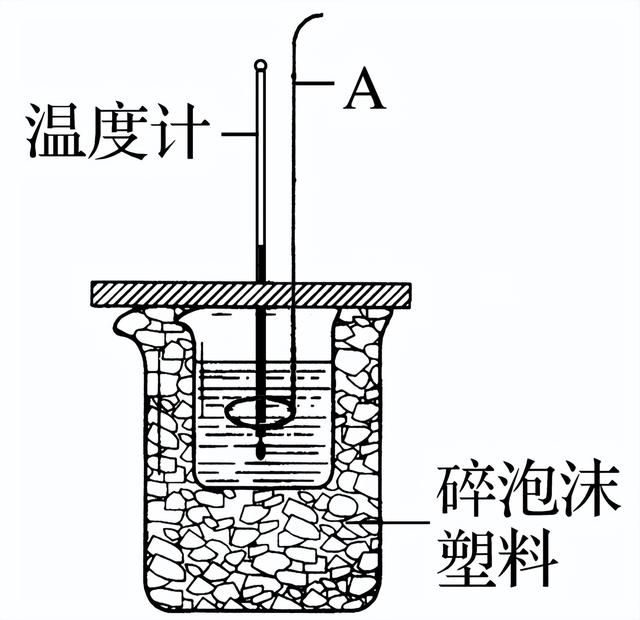
A.稍过量的氢氧化钠是确保盐酸完全反应
B.仪器A的名称是玻璃棒
C.酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,并不断用玻璃棒搅拌
D.用Ba(OH)2和硫酸代替盐酸和NaOH溶液进行反应,结果也是正确的
6.(2020·浙江7月选考,22)关于下列ΔH的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH1
CO(aq)+H2O(l)HCO(aq)+OH-(aq) ΔH2
OH-(aq)+H+(aq)===H2O(l) ΔH3
OH-(aq)+CH3COOH(aq)===CH3COO-(aq)+H2O(l)
ΔH4
A.ΔH1<0 ΔH2<0 B.ΔH1<ΔH2
C.ΔH3<0 ΔH4>0 D.ΔH3>ΔH4
7.(2020·天津市蓟州区月考)下列各组热化学方程式中,ΔH1>ΔH2的是( )
①C(s)+O2(g)===CO2(g) ΔH1
C(s)+O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH1
S(g)+O2(g)===SO2(g) ΔH2
③H2(g)+O2(g)===H2O(l) ΔH1
2H2(g)+O2(g)===2H2O(l) ΔH2
④CaCO3(s)===CaO(s)+CO2(g) ΔH1
CaO(s)+H2O(l)===Ca(OH)2(s) ΔH2
A.① B.②③④
C.④ D.①②
8.(1)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:
①N2(g)+2O2(g)===2NO2(g)
ΔH1=+67.7 kJ·mol-1
②N2H4(g)+O2(g)===N2(g)+2H2O(g)
ΔH2=-534 kJ·mol-1
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:____________________。
(2)氢气的燃烧热为286 kJ·mol-1。写出表示氢气燃烧热的热化学方程式:________________________________________________________________________。
(3)等质量的下列物质分别完全燃烧,反应过程放出热量较多的是________(填选项字母)。
A.固体硫 B.硫蒸气
(4)已知:通常条件下,强酸、强碱稀溶液发生中和反应生成1 mol H2O(l)放出的热量为中和热。稀溶液中1 mol H2SO4和足量NaOH恰好反应时放出Q kJ热量,则其中和热为________kJ·mol-1。
(5)已知H2和O2反应放热,且断开1 mol H—H键、1 mol O===O键、1 mol O—H键吸收的能量分别为Q1 kJ、Q2 kJ、Q3 kJ,由此推知下列关系正确的是____(填字母)。
A.Q1+Q2>Q3 B.Q1+Q2>2Q3
C.2Q1+Q2<4Q3 D.2Q1+Q2<2Q3

免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com